水・空気の物性 密度 粘度 動粘度 機械用語集 > 流体力学 > 水・空気の物性 水・空気の物性 ここでは代表的な流体である、水と空気の物性一覧表を示します。 標準大気圧(MPa)における水・乾燥空気の物性 水 温度 ℃ 密度Jun 09, 13ベストアンサー AgClの100℃での溶解度積ってどういう目的で使用されるのでしょうか。 ネットで検索すると http//wwwndaacjp/~asanoa/lectures/ac/SolutionEquilibriumpdf にありました。 文献は不明ですが。 5℃ x10^ (11) (mol/L)^2 10℃ 40x10^ (11) (mol/L)^2 25℃ 10x10^ (10) (mol/L)^2 50℃ 10x10^ (9) (mol/L)^2 100℃ x10^ (9) (mol/L)^2 溶解熱次に,難溶性の沈殿の生成とそれに対するpHの影響があまり考慮されていない様に思います.例えば,水酸化物の沈殿を生じる場合の反応式と上澄み液中の溶解度積Kspは (13) Fe 3 3OH→ Fe(OH) 3 ↓茶色沈殿 , (14) Ksp1=Fe 3OH 3 ≒3×1038 (mol/L) 4

2 Barasquared C See How To Solve It At Qanda
塩化鉛 溶解度積 100°c
塩化鉛 溶解度積 100°c-塩化亜鉛 ZnCl 2 342 353 395 437 452 4 541 614 塩化アルミニウム AlCl 3 439 449 458 466 473 481 486 490 塩化アンモニウム NH 4 Cl 294 332 372 414 458 504 553 602 656 712 773 塩化イットリウム(III) YCl 3 773 781 7 796 808 塩化インジウム(III) InCl 3 210 212 塩化ウラニル UO 2 Cl 2 3 塩化カドミウム CdCl 2中程度の強度があり、耐食性・溶接性が良い。 一般的な工作に一番向いている材料。 一般工作材料・一般機械材料 一般板金・アルミ船舶・車両・建築材 ×




金属イオンの分離実験の語呂合わせ 17h29大学入学共通テスト試行調査第1回第2問 問2 A B 入試化学を語呂合わせで解く大学入試ゴロ化学
水への溶解度 334 g/100 mL (100 ℃) 融点 501 ℃ 沸点 950 ℃ 塩化鉛 (えんかなまり、lead chloride)は 鉛 の 塩化物 。 鉛の酸化数の違いで塩化鉛 (II) と塩化鉛 (IV) が存在する。Feb 06, °c;たとえば、℃の水100gには、358gまで食塩が溶けます 「 水100gにものが何g溶けるか 」を 溶解度 といいます。 具体例を使って考えてみましょう。 まず、食塩の溶解度は358です。 これは、水100gに食塩が 358g まで溶けるという意味ですね。 もし水が0gあとったすると、食塩は何gま 溶解度は、溶媒100グラムに溶ける溶質の量(グラム数)であらわされます 溶解度
比熱とは1gあたりの物質の温度を1度あげるのに必要な熱量のことです。 つまり、 比熱 とは、物質1gあたりの熱容量ということになります。 比熱は大きくなるほど、温まりにくく、さめにくい性質をもっています。 C=mc (C:熱容量J/K 又は cal/K mタンパク質の水に対する溶解度は塩濃度が薄い間はイオン強度Iに比例し増加するが(I = 01間 塩溶効果)、更に塩濃度が増すと溶解度は(11)式に従い減少する logS = β – K s I (11) S タンパク質溶解度 Ks 各種塩の塩析効果を示す塩析係数(塩類の種類で決まる)(1)AgCl は水に対する溶解度積がAgCl -=16×10 19 mol2dm 6(25℃)の難溶 性塩である.AgCl の溶解度を求める方法に関する以下の設問に答えよ.ただし, 溶液を混合した場合に混合後の体積は混合前の体積の和となるとし,また活量は
時間室温に放置する。沈殿を水洗濾過したのち100。cで乾燥した。 0.2mfe11 ci2溶液に2mウロトロピン溶液を加えてfe(oh)2の沈殿 を析出させたのち,濃hci溶液80 m4と1mnano2溶液を加え 60℃で酸化する。沈殿を水洗濾過したのち60℃で乾燥した。Jan 19, °C;塩化銀の溶解度積 K = 1 問題13:溶解度積・酸化還元反応 塩化銀の溶解度積は97 C において210×1011、室温(25 C)では156×1010 である。 a) 50 C におけるAgCl の溶解度積と溶解度(単位 mg/dm3)を推定せよ。 AgCl は水にはほとんど溶解しないが 三フッ化塩素と反応




2 Barasquared C See How To Solve It At Qanda




入試化学を語呂合わせで解く大学入試ゴロ化学
May 11, 15特開(PA) IP Force 特許公報掲載プロジェクト β版塩化亜鉛 ZnCl 2 342 353 395 437 452 4 541 614 塩化アルミニウム AlCl 3 439 449 458 466 473 481 486 490 塩化アンモニウム NH 4 Cl 294 332 372 414 458 504 553 602 656 712 773 塩化イットリウム(III) YCl 3 773 781 7 796 808 塩化インジウム(III) InCl 3 210 212 塩化ウラニル UO 2 Cl 2 3 塩化カドミウム CdCl 2Oct 25, 08また、温度を100℃にするとどうなるか。 ただし PbCl2 の25℃と100℃における溶解度積はそれぞれ 16*10^5 と 47*10^4 とする。




Dviout 気体と溶 Pdf 無料ダウンロード




入試化学を語呂合わせで解く大学入試ゴロ化学
塩化銀を溶解 し 銀イオンと塩を形成したときの溶解度積が塩化 neutralizing only one portion of the entire amount of negative charges of the zeolite with a silver ion, and drying at 100 °C or lower temperature under ordinary pressure 特許庁水への溶解度 447 g/L (25 C) 107 g/L (100 C) 溶解度 フッ化水素酸、塩酸に不溶 その他の酸やアルカリに可溶 屈折率 (n D) 1650 構造 結晶構造 六方晶 危険性 EU Index Not listed 引火点 (不燃性) 半数致死量 LD 50 3700 m 第3 章では、気体のHansen溶解度パラメータに関する研究結果について検討し3.2 塩化銀の溶液度積 方法 (1)に従っ て作成した滴定曲線を図1に示す。 溶液量が多く銀濃度が薄い ため当量点付近での電位 の変化が小さく滴定結点がわかりに くい。滴定終点の 決定法にはい くつ かの方法があるが , ここではグラン



第116章 溶解平衡




Dviout 気体と溶 Pdf 無料ダウンロード
塩mx の溶解度積よりも きければ、mx の沈殿が析出し、 さければ沈殿は じ ない。共通イオン効果 •沈殿mx が存在している 溶液に、さらにxを 加えてx を きくすると、溶解度積の値を保 つために、m が さくなるようにmx が沈殿 塩化鉛の溶解度はTs en 鉛蓄電池 始動用 パート4:大型車両用アキュムレータの寸法 ts en ランプホルダー バヨネット ts en 火災危険度試験 パート115:試験炎 針炎試験方法 装置、検証試験の設定および手引きFeb 06, °C;




14 号 酸素発生用陽極及びその製造方法 Astamuse




セット割 理論化学ドリルシリーズ全巻セット 化学のグルメオンラインストア
赤羽政亮・矢野弘子 SiO2NaOH水溶液とMgCl2水溶液との反応につき,℃ ,および100℃で実験した。 反応後の水溶液の分析結果より,最初のNaOH/SiO2のモル比(以下Na/Si比と記す)が一定のときは,MgCl2の添 加量がNaOHと当量になるまではケイ酸濃度は急激に減少するが,MgCl2が過剰になってもほとんど変化がない。 固相中のMg/Si比(モル比)を計算すると,Na/Si比のほぼ1/2であり,ケイ酸温度 密度 粘度 音速 温度 密度 粘度 音速 ℃ kg/m 3 mPa・s m/sec ℃ kg/m 3 mPa・s m/sec 435 510 9872.71×10-8 Ksp(PbI2)はほぼ一定になりましたね。 それでは考察です。 ℃におけるヨウ化鉛(II)の溶解度は,水100gに対して6.0×10-2gである。 溶解度積は,PbI2の式量=461だから,飽和溶液におけるヨウ化鉛(II)の物質量=6.0×10-2/461〔mol〕。 したがって,飽和溶液100+6.0×10-2〔g〕の体積を100mL とすると,モル濃度=6.0×10-2/461×1000/100



セレン 水浄化フォーラム 科学と技術




電子版 理論化学ドリルシリーズ 化学 化学のグルメオンラインストア
基礎講座|精密ポンプ技術 62 液体の気化(蒸発) 液体の気化(蒸発) 前項の「71 キャビテーションについて」のビールの例は、液中に溶けていた炭酸ガスが圧力の低下に伴って液の外に逃げ出すことを示していました。6 Specified for use over an extended temperature range 223 K (– 50 °C) to 373 K (100 °C) or specified as suitable for aerospace applications Note 329b includes xenon flashlamp drivers 330 Highspeed pulse generators, and 'pulse heads' therefor, having both of the following characteristics a難溶解性物質は,常温から高温(100°c)において水 にほとんど溶解しないか,加水分解により不溶性化合物 を形成すると考えられるが,数100~1100°c の過熱水 蒸気で処理すれば分解できる。この方法は熱加水分解法




塩化銀 I Wikipedia




Wo18 号 酸化物ナノシート及びその製造方法 Astamuse
塩化ニッケル 溶解度 3 55 g/cm 3, 固体(無水物) 水への溶解度 254 g/100 mL ( ℃) 融点 1001 ℃ 塩化ニッケル (II) (えんかニッケル (II)、nickel (II) chloride)は 塩素 と ニッケル のイオン性化合物( 塩 )である。 無水物の組成式は NiCl 2 で、融点の高い常磁性を持つ黄色の固体である。 ニッケル化合物としては最も広く使われており、ニッケルめっきなどに用いJan 25, 1998社団法人 資源・素材学会 A hydrolysis reaction was carried out by adding a certain amount of zinc oxide into the sulphuric acid acidified ferric sulphate solutions with various concentrations at 70 °C, 80 °C, 90 °C, 100 °C and 110 °C respectively for more than 168 hours The composition of solutions and the precipitation of goethite, which were balanced with solutions at塩化銀えんかぎんsilver chloride 普通は AgC l をさす。 無色の 粉末 で光に当てると黒変する。 比重 556,融点 455℃,沸点 1550℃。 水に難溶で, 溶解度 は 10℃で 08mg/ l ,100℃で 217mg/ l 。 しかし,濃塩酸,アンモニア水にはそれぞれ錯イオン AgCl 2 , Ag (NH 3) 2 をつくって溶ける。 またシアン化アルカリ, チオ硫酸塩 ,炭酸アンモニウムの溶液にも 類似 の反応




金属イオンの分離実験の語呂合わせ 17h29大学入学共通テスト試行調査第1回第2問 問2 A B 入試化学を語呂合わせで解く大学入試ゴロ化学



質問箱
シアン化亜鉛 zn(cn) 2 0058 シアン化カドミウム cd(cn) 2 0022 シアン化カリウム kcn 50 シアン化カルシウム ca(n 3) 2 45 シアン化銀 agcn 1467e07 シアン化水銀(i) hg 2 (cn) 2 2266e12 シアン化水銀(ii) hg(cn) 2 93 シアン化タリウム(i) tlcn 168 シアン化銅(i) cucn 1602e09 シアン化ナトリウム nacn 408 481 587JPH0698A JPA JPA JPH0698A JP H0698 A JPH0698 A JP H0698A JP A JP A JP A JP Aタイトル 平成23年台風12号浸水災害時の紀宝町における自主防災活動の実態 著者 岡島賢治・酒井俊典・古根川竜夫
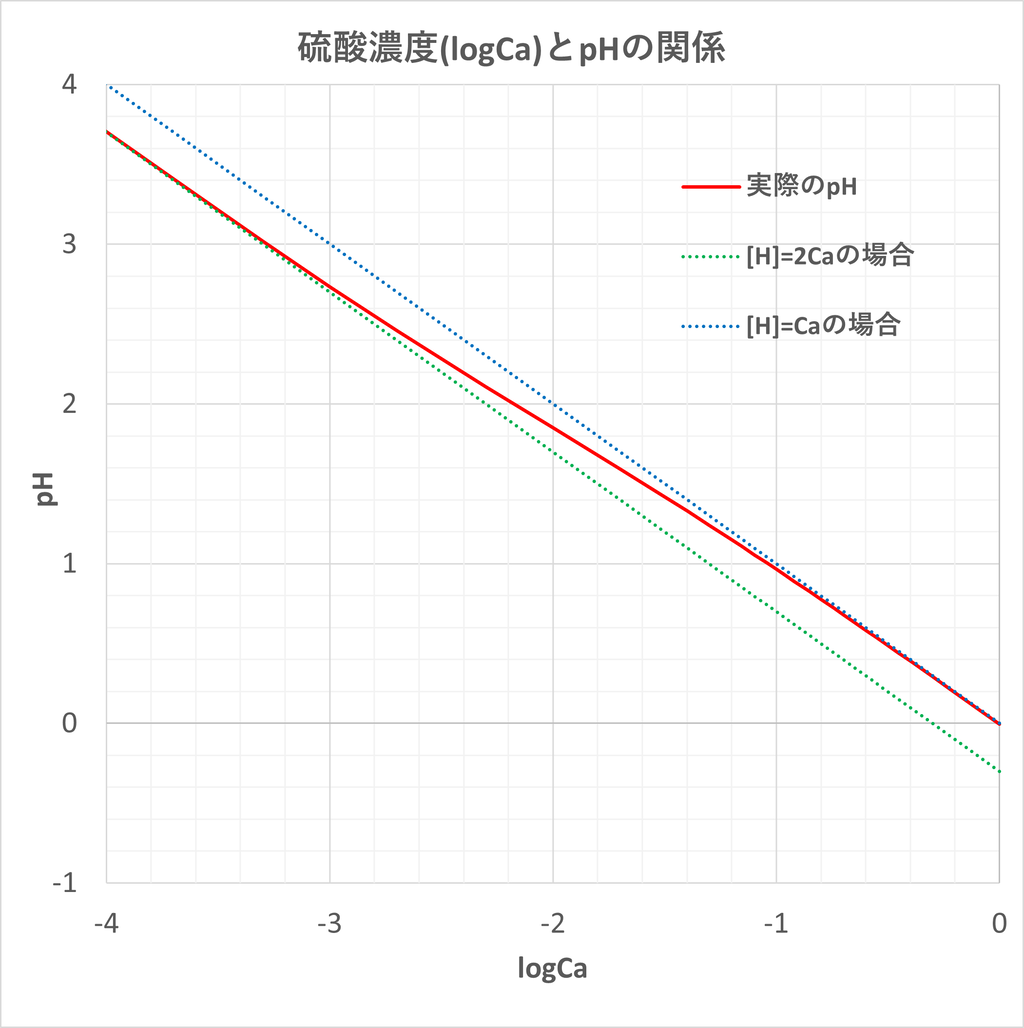



活量係数 滴定曲線 溶解度などーエクセルを用いて




Pdf Suppression Of Silver Dissolution By Contacting Different Metals During Copper Electrorefining
請求項1〜5記載のフォトポリマー組成物を溶剤に溶解させ、得られた溶液を基板上に塗布し、その後、溶剤を揮散させ記録層を形成する請求項6記載のホログラム記録媒体の製造法。 発明の詳細な説明 技術分野 0001@ 単価で/につき 104 通信で用いられる『了解』の意を表す語 A answer / ampere a about / acres / adjective - (地質の年代で)三畳トップ > 化学 ii > 第 2 部 反応速度と平衡>第 2 章 化学平衡> 第 3 節 電離平衡 第 3 節 電離平衡 電離平衡 溶液中における溶質分子と,それらが電離して生じるイオンとの間の平衡状態を いう。一般に,弱電解質の水溶液中における電離平衡では,質量作用の法則がよく




Images Of 溶解度積 Japaneseclass Jp




Dviout 気体と溶 Pdf 無料ダウンロード
金属塩化物の溶解度 ※ ここで示す「溶解度」は、飽和溶液100gに含まれる溶質のグラム数です。 塩化物 化学式 0℃ ℃ 40℃ 60℃ 80℃Sep 15, 19Substance name 硝酸鉄 (III) Iron (III) nitrate 化学式 Chemical formula Fe (NO 3) 3 外観 Appearance 薄菫色の固体




セット割 化学のグルメ問題集全巻セット 化学のグルメオンラインストア



2 Barasquared C See How To Solve It At Qanda



高校生の化学




ヨウ化鉛 Ii Wikipedia



1 K 18times10 10 Mom 2 Lihat Cara Penyelesaian Di Qanda




1 K 18times10 10 Mom 2 Lihat Cara Penyelesaian Di Qanda




21 号 硫黄 炭素複合体 その製造方法 及びこれを含むリチウム二次電池 Astamuse




14 号 電極体 及び当該電極体を備える電池 Astamuse




Pdf Influence Of Chloride Ions On Quality And Mechanical Properties Of Electrodeposited Copper In Copper Electrorefining




Pdf Removal Of Fluoride From Wastewater Of Hot Spring By Hydroxyapatite Synthesized From Gypsum Waste And Its Optimum Treatment




電子版 セット割 全巻セット 化学のグルメオンラインストア




16 号 水から材料を分離するためのシステム 装置及び方法 Astamuse




問1なのですが解法を見てもさっぱりわかりません なぜcl のモル濃度を求めた後に溶解 Clear



3ページ目の 共通テスト解説 とある化学教師でググって 楽天ブログ




問1なのですが解法を見てもさっぱりわかりません なぜcl のモル濃度を求めた後に溶解 Clear




Dviout 気体と溶 Pdf 無料ダウンロード
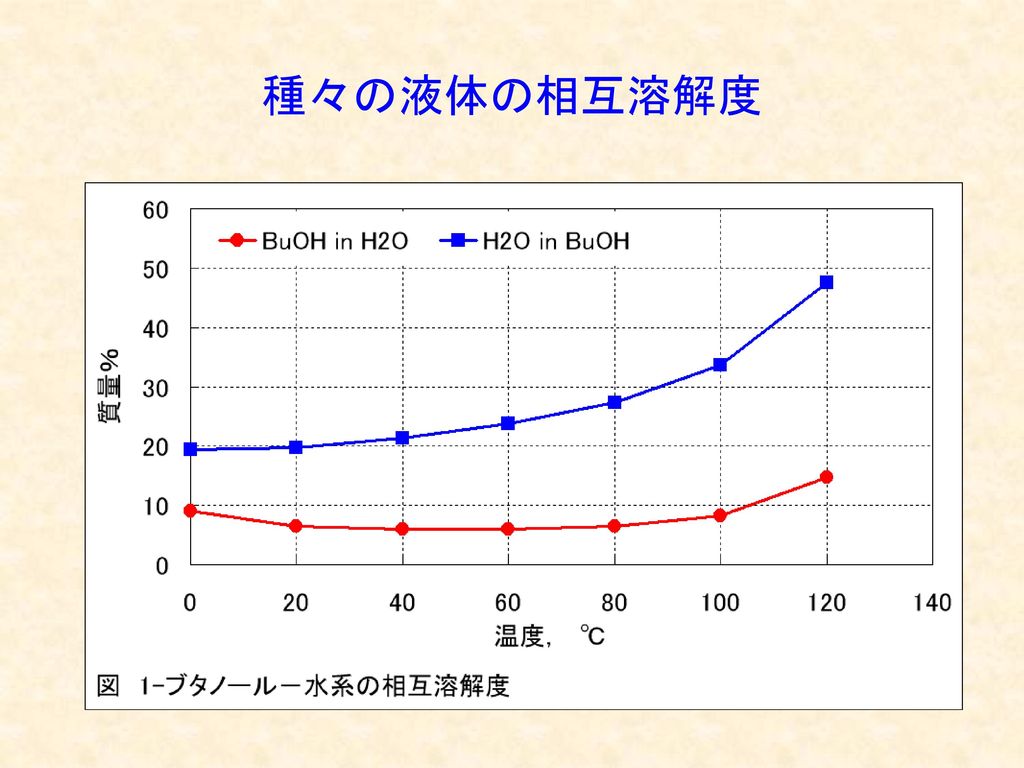



溶解 酸化 還元 酸 塩基 埼玉大学 教育学部 理科教育講座 芦田 実 Ppt Download




1 K 18times10 10 Mom 2 Lihat Cara Penyelesaian Di Qanda




Woa1 ニッケル マンガン系複合酸化物及びその製造方法 並びにその用途 Google Patents




問1なのですが解法を見てもさっぱりわかりません なぜcl のモル濃度を求めた後に溶解 Clear




2 Barasquared C See How To Solve It At Qanda
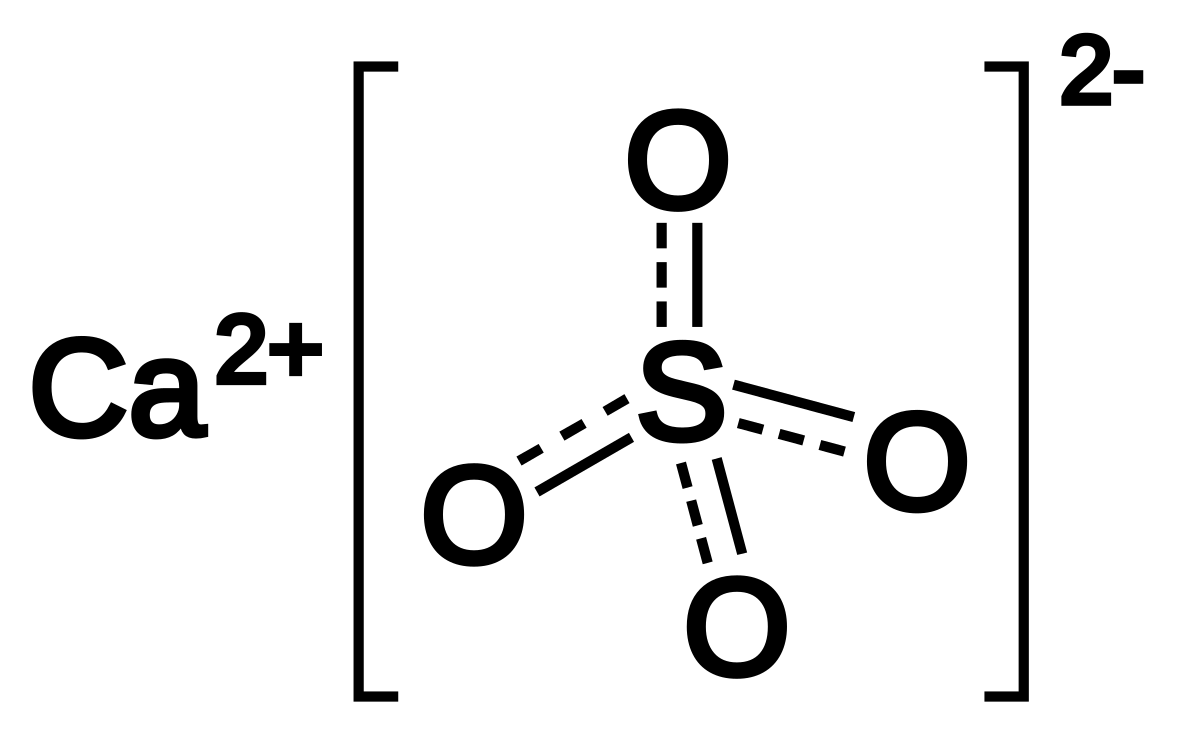



硫酸カルシウム Wikipedia


